Пре него што започнемо директно упознавање концепата повезаних са оловном батеријом, кренимо од њене историје. Дакле, француски научник по имену Ницолас Гаутхерот 1801. године приметио је да у испитивањима електролизе постоји минимална количина струје чак и када постоји искључење главне батерије. Док је 1859. године научник Гатсон развио оловно-киселу батерију и ово је била прва која се пуни проласком обрнуте струје. Ово је била почетна верзија ове врсте батерија, док је Фауре затим додао многа побољшања и на крају је практични тип оловне киселине изумио Хенри Тудор 1886. године. Хајде да детаљније разговарамо о овој врсти батерија. батерија , рад, врсте, конструкција и предности.
Шта је оловна киселина?
Оловне киселине спадају у класификацију пуњивих и секундарних батерија. Упркос минималним пропорцијама батерије у запремини и енергији у тежини, она има способност да испоручује повећане ударне струје. То одговара томе што ћелије оловне киселине поседују велику количину снаге према тежинским пропорцијама.
То су батерије које користе оловни пероксид и сунђерасто олово за претварање хемијске енергије у електричну. Они су углавном запослени у трафостаницама и електроенергетским системима из разлога што имају повећани ниво напон ћелије и минималне трошкове.
Конструкција
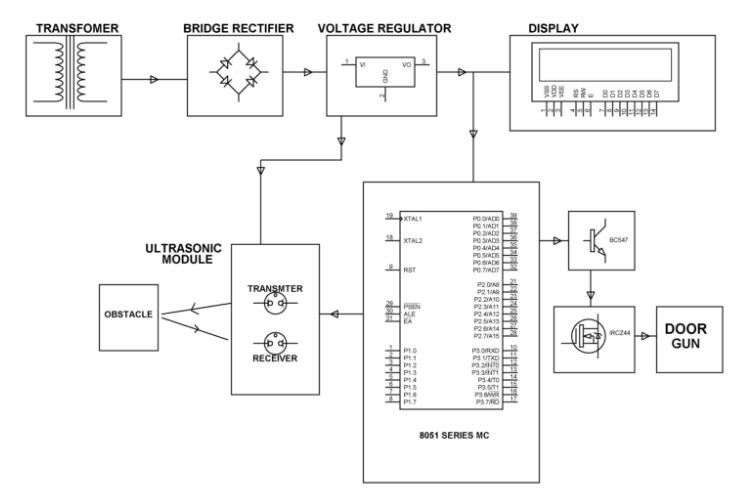
У конструкција оловних батерија , плоче и контејнери су кључне компоненте. Доњи одељак пружа детаљан опис сваке компоненте коришћене у конструкцији. Тхе дијаграм оловних батерија је

Контејнер
Овај део контејнера израђен је од ебонита, дрвета обложеног оловом, стакла, тврде гуме направљене од битуменског елемента, керамичких материјала или коване пластике који су постављени на врх да би се елиминисала било каква пражњења електролита. Док у доњем делу контејнера постоје четири ребра, где су два постављена на позитивну плочу, а друга на негативну плочу.
Овде призма делује као основа за обе плоче, а додатно штити плоче од кратког споја. Компоненте које се користе за израду контејнера не би смеле да садрже сумпорну киселину, не би требало да се савијају или пропусте и да не садрже нечистоће што доводи до оштећења електролита.
Плоче
Плоче у оловној батерији су направљене на другачији начин и све су сачињене од сличних врста мреже која је изграђена од активних компоненти и олова. Мрежа је кључна за успостављање проводљивости струје и за ширење једнаких количина струја на активне компоненте. Ако постоји неравномерна расподела, тада ће доћи до попуштања активне компоненте. Плоче у овој батерији су две врсте. То су плоче од планте / обликоване плоче и Фауре / залепљене плоче.
Формиране плоче се углавном користе за статичке батерије, а имају и тешке и скупе батерије. Али они су дуготрајни и нису склони да изгубе своје активне компоненте чак и у континуираним процесима пуњења и пражњења. Имају минималан капацитет према тежини.
Док се лепљени поступак углавном користи за израду негативних плоча него позитивних плоча. Негативна активна компонента је донекле компликована и они доживљавају благе модификације у процесима пуњења и пражњења.
Активна компонента
Компонента која активно учествује у процесима хемијске реакције који се дешавају у батерији углавном у време пуњења и пражњења назива се активном компонентом. Активне компоненте су:
- Оловни пероксид - Твори позитивну активну компоненту.
- Спужвасто олово - Овај материјал формира негативну активну компоненту
- Разблажена сумпорна киселина - Ово се углавном користи као електролит
Сепаратори
То су танке плоче израђене од порозне гуме, обложеног оловног дрвета и стаклених влакана. Одвајачи су постављени између плоча како би се обезбедила активна изолација. Имају жлебљени облик на једној страни и глатку завршну обраду на другим ивицама.
Ивице батерије
Има позитивне и негативне ивице пречника 17,5 мм и 16 мм.
Принцип рада оловне киселине
Како се сумпорна киселина користи као електролит у батерији, када се она раствори, молекули у њој се распршују у облику СО4-(негативни јони) и 2Х + (позитивни јони) и они ће имати слободно кретање. Када се ове електроде умоче у растворе и обезбеде напајање једносмерном струјом, тада ће се позитивни јони кретати и кретати према смеру негативне ивице батерије. На исти начин, негативни јони ће се кретати и кретати према смеру позитивне ивице батерије.
Сваки водоник и сулфатни јони сакупљају по један и двоелектронски и негативни јон са катоде и аноде и они реагују са водом. Ово ствара водоник и сумпорну киселину. Док развијене од горе наведених реакција реагују са оловним оксидом и формирају оловни пероксид. То значи да у тренутку процеса пуњења оловни катодни елемент остаје сам као олово, док се оловна анода формира као оловни пероксид који је тамно смеђе боје.
Кад нема ДЦ напајање а онда у тренутку када је волтметар повезан између електрода, он приказује потенцијалну разлику између електрода. Када постоји веза жице између електрода, доћи ће до проласка струје са негативне на позитивну плочу преко спољног кола што значи да ћелија има способност да обезбеди електрични облик енергије.
Дакле, ово показује оловна батерија ради сценарију.
Различити типови
Тхе типови оловних киселина углавном су категорисани у пет типова и они су детаљно објашњени у наставку.
Поплављени тип - Ово је уобичајени тип паљења мотора и има вучну батерију. Електролит има слободно кретање у ћелијском делу. Људи који користе овај тип могу имати приступ свакој ћелији и могу додати воду у ћелије када се батерија исуши.
Запечаћени тип - оваква оловна батерија је само мала промена на поплављеном типу батерија. Иако људи немају приступ свакој ћелији у батерији, унутрашњи дизајн је готово сличан оном преплављеном типу. Главна варијација овог типа је да постоји довољна количина киселине која издржава несметан проток хемијских реакција током трајања батерије.
ВРЛА тип - Они су позвани Батерије са оловном киселином које регулишу вентили који се такође називају и заптивеним типом батерија. Поступак контроле вредности дозвољава сигуран развој О.дваи Х.двагасови у време пуњења.
АГМ Типе - Ово је акумулаторска батерија која апсорбује стакло која омогућава заустављање електролита у близини материјала плоче. Ова врста батерије повећава перформансе процеса пражњења и пуњења. Они се посебно користе у апликацијама за моторе и покретање мотора.
Тип гела - Ово је мокра врста оловне киселине, у којој је електролит у овој ћелији повезан са силицијевим диоксидом, што чини укрућење материјала. Вредности напона пуњења ћелије појеле су се минимално у поређењу са другим типовима и такође имају већу осетљивост.
Хемијска реакција оловне батерије
Хемијска реакција у батерији се углавном дешава током метода пражњења и пуњења, а у процесу пражњења објашњава се на следећи начин:
Када се батерија потпуно испразни, анода и катоде су ПбОдваи Пб. Када се споје помоћу отпора, батерија се празни, а електрони имају супротан пут у време пуњења. Тхе Хдвајони се крећу ка аноди и они постају атом. Долази са ПбОдва, чиме се формира ПбСО4која је беле боје.
На исти начин, сулфатни јон се креће према катоди и након достизања, јон се формира у СО4. Реагује са оловом катода стварајући тако оловни сулфат.
ПбСО4+ 2Х = ПбО + ХдваИЛИ
ПбО + Х.дваТАКО4= ПбСО4+ 2ХдваИЛИ
ПбОдва+ ХдваТАКО4+ 2Х = ПбСО4+ 2ХдваИЛИ

Хемијске реакције
Током процеса пуњења, катода и аноде су у вези са негативним и позитивним ивицама истосмерног напајања. Позитивни јони Х2 крећу се у смеру катоде и добијају два електрона и формирају се као атом Х2. Подвргава се хемијској реакцији са оловним сулфатом и формира олову и сумпорну киселину.
ПбСО4+ 2ХдваО + 2Х = ПбСО4+ 2 Х.дваТАКО4
Комбинована једначина за оба процеса представљена је као

Процес пражњења и пуњења
Овде стрелица надоле означава пражњење, а стрелица нагоре поступак пуњења.
Живот
Оптимална функционална температура оловних батерија је 250Ц што значи 770Ф. Повећање опсега температуре скраћује дуговечност. По правилу, за сваких 80 ° Ц пораста температуре смањује време полураспада батерије. Док је батерија регулисана вредношћу која функционише на 250Ц има а век трајања оловне киселине од 10 година. А када се ово оперише у 330Ц, има животни период од само 5 година.
Апликације за оловне киселине
- Они се користе у осветљењу за случај нужде да би обезбедили напајање пумпи са јастуцима.
- Користи се у електромоторима
- Подморнице
- Нуклеарне подморнице
Овај чланак је објаснио принцип рада оловне киселинске батерије, врсте, век трајања, конструкцију, хемијске реакције и примену. Поред тога, знајте шта су предности оловних батерија и недостаци у разним доменима?